 Заряженный аккумулятор способен сохранять накопленную электрическую энергию длительное время. Заряженный аккумулятор способен сохранять накопленную электрическую энергию длительное время.
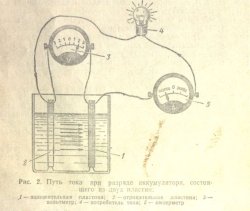
При разряде аккумулятора (рис. 2) значительная часть двуокиси свинца на положительной и губчатого свинца на отрицательной пластинах превращается в сульфат свинца. Процесс образования сульфата свинца при разряде аккумулятора сопровождается понижением плотности электролита.
Химические реакции, протекающие при разряде и заряде аккумуляторов, можно представить так:
До разряда Разряд После разряда
РbO2 + Pb + 2H2S04 = PbS04 + PbS04 + 2H20
Количество электрической энергии, которое может накопить и отдать аккумулятор, зависит от количества активной массы, участвующей в электрохимической реакции, от температуры электролита, от величины разрядного тока и времени разряда.
Основные величины, характеризующие свойства аккумуляторной батареи,— электродвижущая сила, напряжение и отдаваемая емкость.
3. Электродвижущая сила (ЭДС) — это разность потенциалов 1 положительных и отрицательных пластин (без токовой нагрузки). Зависит ЭДС в основном от плотности электролита, находящегося в данный момент в аккумуляторе.
Величина электродвижущей силы аккумулятора может быть определена по эмпирической формуле
Eа = 0,84 + т(в),
где E а =ЭДС аккумулятора,
у—плотность электролита (при +15° С в аккумуляторе). По показаниям вольтметра при отсутствии тока нагрузки нельзя судить о степени заряженности (или разряженности) аккумуляторной батареи. В отличие от напряжения электродвижущая сила измеряется вольтметром при разомкнутой внешней цепи, т. е. без тока нагрузки. Практически ЭДС измеряется для обнаружения Короткого замыкания между пластинами. При неполном коротком замыкании ЭДС аккумулятора будет ниже, чем в исправном аккумуляторе, а при полном коротком замыкании она становится равной нулю.
|